
Regie op registers: onderweg naar nieuw doelmatigheidsonderzoek van geneesmiddelen
Nieuwe geneesmiddelen vinden hun weg naar de medische praktijk via klinische trials. Op basis van die trials weten we wat het effect is van de behandeling en welke bijwerkingen kunnen ontstaan bij een bepaalde groep patiënten. Echter, effectiviteit en toxiciteit kunnen in de dagelijkse klinische praktijk afwijken ten opzichte van de trials. Hoe kunnen we de effectiviteit van geneesmiddelen in de dagelijkse praktijk beter beoordelen? IKNL is samen met de Dutch Colorectal Cancer Group (DCCG) betrokken bij het project ‘Regie op Registers voor Dure Geneesmiddelen’ van Zorginstituut Nederland, dat op die vraag antwoord wil geven.
Het project richt zich op een informatielandschap waarin praktijkinformatie over dure geneesmiddelen wordt vastgelegd in aandoeningsspecifieke registraties. Daardoor ontstaat de mogelijkheid om te leren van de werking van dure geneesmiddelen in de praktijk. 'Onderdeel van dit project zijn vier casestudies, waarin het gebruik van registers voor pakketbeheer vanuit verschillende perspectieven wordt belicht’, vertelt Heidi van Doorne, adviseur bij IKNL. ‘Wij kijken in een van de casestudies samen met de Dutch Colorectal Cancer Group (DCCG) naar de effectiviteit van twee middelen voor de behandeling van darmkanker in de dagelijkse praktijk: encorafenib in combinatie met cetuximab(*). Het zijn middelen die relatief duur zijn en gepaard kunnen gaan met toxiciteit: je wilt ze dus inzetten voor de patiënten die hier écht baat bij hebben. Daarmee is de patiënt het beste geholpen, en jagen we de zorg niet op onnodige kosten. Onze casestudie heeft het doel om het Zorginstituut te helpen met inzichten over welke gegevens moeten worden verzameld en op welke manier. We beantwoorden vragen als: hoe bepaal je de effectiviteit van een (nieuw) geneesmiddel in de praktijk? Waar loop je tegen aan? Welke items heb je nodig uit welke registers? Hoe kun je die bronnen aan elkaar verbinden? En vooral: hoe maak je zo optimaal mogelijk gebruik van bestaande registers en beperk je de registratielast van zorgverleners?’
Eenheid van taal
‘Binnen deze casestudie hebben we rond de 40 items nodig om de vraagstelling goed te kunnen beantwoorden’, vertelt klinisch informaticus Patrick Lubbers. ‘Die items komen uit verschillende databases: de Nederlandse Kankerregistratie, PROFIEL, PLCRC, Dutch Hospital Data en epd’s. Om deze data te kunnen analyseren, zullen we moeten zorgen dat de items als het ware in dezelfde taal zijn geschreven.’ Die koppeling is op veel plekken al mogelijk, maar tegelijk ziet Lubbers nog uitdagingen. ‘Het kan technisch heel goed mogelijk zijn om bijvoorbeeld items over de toxiciteit uit de systemen te halen, de data moeten dan wel aanwezig zijn. Bij de uitvraag van data rondom toxiciteit zien we dat dat niet altijd het geval is. Waarnemingen staan bijvoorbeeld in vrije tekstvelden van de epd’s, en zijn daarmee een stuk lastiger te extraheren en te koppelen aan andere databronnen. Daarin moeten we een goede afstemming zoeken met zorgverleners zelf. Het kan immers volkomen logisch zijn dat de informatie technisch gezien niet op de juiste plek wordt geregistreerd: in beperkte tijd wil je aandacht hebben voor een patiënt, en niet voor de invulvelden op het scherm.’
Uitwisselbaarheid epd’s en governance
Buiten de uitdagingen rond het registreren zelf ziet Lubbers ook dat de verschillende epd’s die in Nederlandse ziekenhuizen worden gebruikt niet altijd helpen. ‘Het ene epd kan net weer anders ingericht zijn dan het andere. Eenheid van taal daarin maakt het verzamelen en analyseren van data eenvoudiger, en dat is iets dat vraagt om centrale regie.’ Van Doorne: ‘Die regie hangt weer samen met de governance. Wie is eigenaar van de data en wie bepaalt hoe deze gestandaardiseerd, geregistreerd en geduid worden? Het antwoord op die vraag is niet eenvoudig te geven, en daarover zijn veel partijen in gesprek.
Actualiteit
Een ander aspect wat speelt is hoe actueel de data moeten zijn bij het beantwoorden van effectiviteitsvraagstukken. Lubbers: ‘Hoe complexer een onderzoeksvraag is, hoe meer er verzameld en geanalyseerd moet worden, en dat kost meer tijd. Data over incidentie geven we in de monitor oncologische zorg op maandniveau, maar data over stadiëring loopt weer iets achter. Dat heeft ook te maken met handmatige registratie van datamanagers van IKNL, omdat eenheid van taal ontbreekt.’ Van Doorne: ‘Vanuit doelmatigheid wil je graag zo actueel mogelijke data, maar tegelijk dat deze kloppend is. Dus het is zoeken naar de juiste balans. Vanuit IKNL werken we aan het project RHONDA, waarin actuele data bijna real time teruggekoppeld wordt. Die inzichten kunnen we ook meenemen in het advies van deze casestudie.’
Patiënt journey
Naast het vraagstuk hoe de data te verzamelen en te verbinden speelt ook de vraag hoe de uitkomsten gepresenteerd kunnen worden. Anja van Gestel, die vanuit IKNL als clinical data scientist bij de casestudie betrokken is: ‘Binnen de casestudie hebben we verschillende gegevenssets onder elkaar gezet. Dat leidde tot zo’n grote brei van informatie dat je door de bomen het bos niet meer kunt zien. Denk aan informatie over chirurgie, verschillende systemische therapieën, behandelepisodes, eerste- en tweedelijnsbehandelingen en tijdstippen waarop PROM-data zijn uitgevraagd. Dat kunnen allemaal belangrijke kenmerken zijn om bijvoorbeeld een inschatting te maken hoe een patiënt reageert op een behandeling. Om die data inzichtelijk te maken, werken we een visualisatie uit in een patient journey. “Dit is een mooi voorbeeld hoe data meer tot leven kan komen. Een dergelijke visuele vertaling is een interessante optie om verder met zorgverleners te verkennen.”
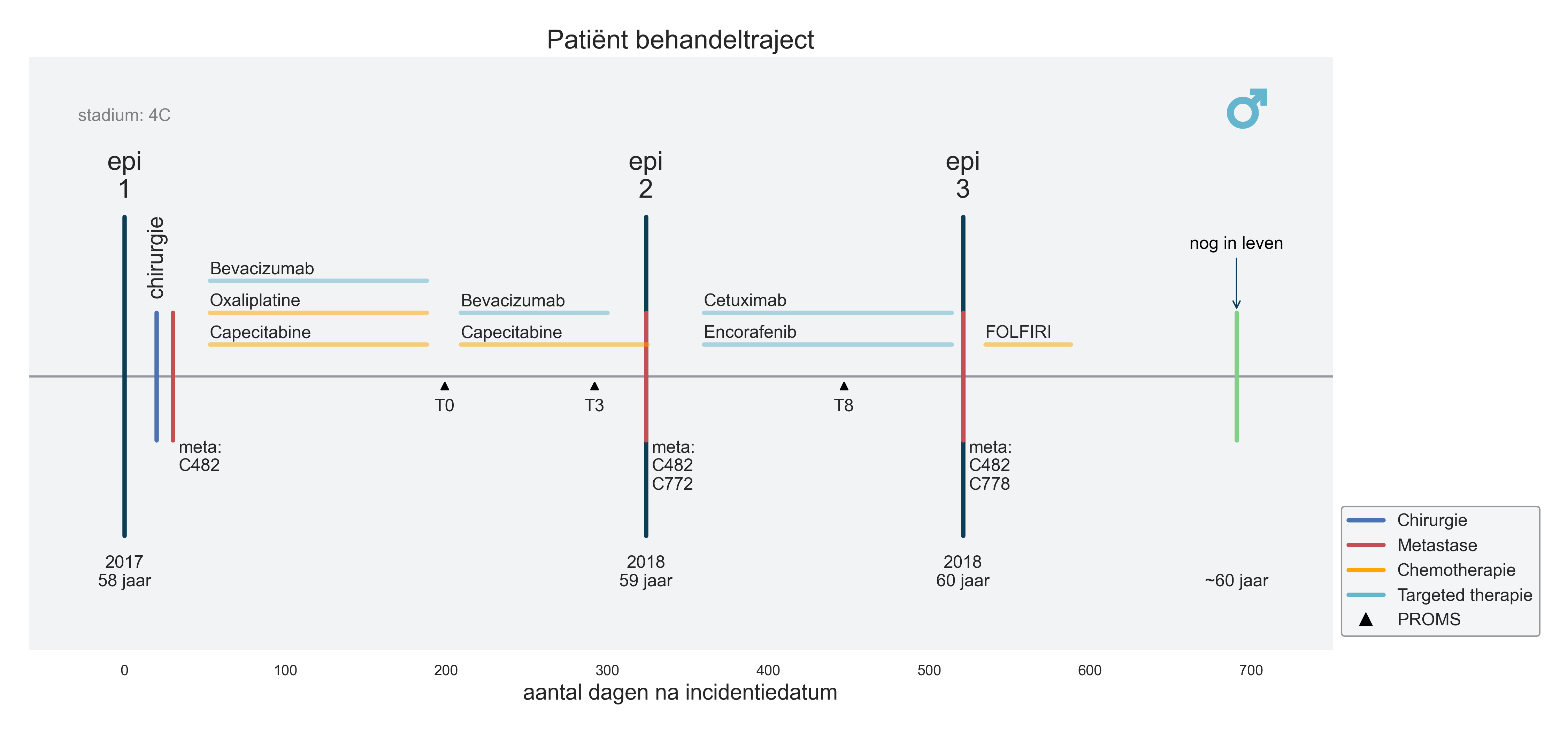
Voorbeeld van visualisatie in patient journey (aan de hand van fictieve data)
Aan het eind van het jaar zal de projectgroep een adviesrapport aanleveren bij het Zorginstituut, met alle kennis die in het project is opgedaan over de voorwaarden en mogelijkheden om gegevens uit registers te gebruiken voor pakketbeheer.
(*) de middelen uit de casestudie kunnen worden ingezet bij volwassen patiënten met BRAFV600E-gemuteerd gemetastaseerd colorectaal carcinoom (mCRC) die eerder zijn behandeld met systemische therapie

.jpg?width=5175&height=3451&ext=.jpg)

